溶媒、官能基ごとに作成した検量線からpKa未知の化合物に対する予測が可能
概要
酸解離定数(pKa)は酸の強さ(プロトンの解離しやすさ)を定量的に表した指標の一つです。pKaが分かることで、pHに対する化合物の溶解性やその状態、医薬品の生体内での吸収されやすさ、pH緩衝作用などの推測に役立ちます。本資料では量子化学計算により得られる酸解離エネルギー差とpKa実験値を用いて、溶媒、官能基ごとに検量線を作成し、分子内水素結合がpKaに与える影響を調べた事例を紹介します。本手法によりpKa未知の化合物に対する予測が可能です。
データ
検量線(pKa実験値[1-8] vs プロトン解離に伴うギブズ自由エネルギー差計算値ΔG)
カルボン酸(20種)
pKa = 0.23ΔG – 59.68
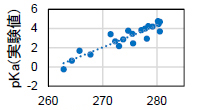
ΔG(計算値) / kcal mol-1
フェノール類(20種)
pKa = 0.21ΔG – 51.44
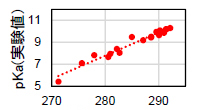
ΔG(計算値) / kcal mol-1
※ pKa = k ΔG + C0
(k, C0は溶媒、官能基ごとに異なるパラメータ)の関係に基づいて検量線を作成[1]
※ 酸解離反応HA ↔ H+ + A-において、ΔG = G(A-) – G(HA)
※ 水溶媒中でのpKa値となります
分子内水素結合がpKaに与える影響
サリチル酸のカルボン酸、フェノール部位のプロトンが順に解離する二段階の反応に着目
aではフェノールOHがCOO–と水素結合を強化しやすく、安定化
→ フェノール部位のプロトンが解離しにくくなり、二段階目のpKa値が上昇
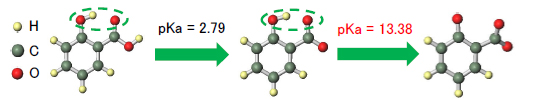
a: 水素結合あり
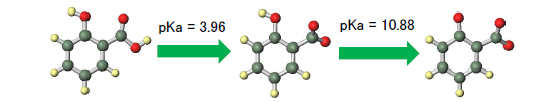
b: 水素結合なし
分子内水素結合により、pKa値が2.5程度変化しうることが示唆
◎分子内水素結合がpKaに与える影響を調べることが可能
◎計算とpKaの実験値から溶媒、官能基ごとに検量線を作成することで、pKa未知の化合物に対する予測が可能
[1] T. Matsui, et al., J. Comput. Jpn., Vol. 15, No. 5 (2016) 184-191.
[2] J. March, Advanced Org. Chem., 3rd Ed. (1985) Unpublished results of W. P. Jencks.
[3] H.C. Brown, et al., in Braude, E.A. and F.C. Nachod Determination of Organic Structures by Physical Methods, Academic Press, New York (1955).
[4] R.M.C. Dawson, et al., Data for Biochemical Research, Oxford, Clarendon Press (1959).
[5] J. Bjerrum, et al., Stability Constants, Chemical Society, London (1958).
[6] O. Gawron, et al., Anal. Chem. 24 (1952) 969.
[7] V.E. Bower, et al., JPC 64 (1960) 1078.
[8] http://www.fm.ehcc.kyoto-u.ac.jp/pKa_compilation_Williams_RipinEvans.pdf